Keywords
σ-дырки
метилтиолированные бензолы
некаталитическое метилтиолирование
согласованное SNAr
сродство к электрону
триазидобензолы
Abstract
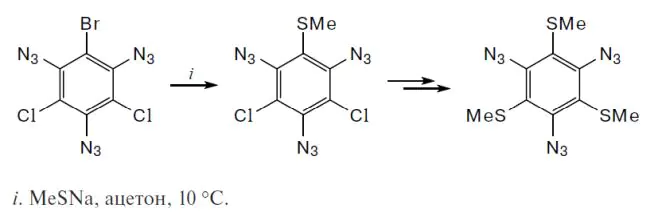
Трибром-, трихлор- и бром(дихлор)замещенные 1,3,5-триазидобензолы реагируют с метилтиолат-анионом в ацетоне при 10 °С по механизму согласованного замещения (сSNAr) с образованием 1,3,5-триазидо-2,4-дибром-6-(метилтио)бензола, 1,3,5-триазидо-2,4-дихлор-6-(метилтио)бензола, 1,3,5-триазидо-2-бром-4,6-ди(метилтио)бензола, 1,3,5-триазидо-2-хлор-4,6-ди(метилтио)бензола и 1,3,5-триазидо-2,4,6-три(метилтио)бензола. Реакции протекают тем легче, чем выше положительный заряд на атомах галогенов и отрицательный заряд на атомах углерода в реакционных центрах C—Hal исходных азидов.
References
1.

Bräse S., Gil C., Knepper K., Zimmermann V.
Angewandte Chemie - International Edition,
2005
2.
S. Bräse, K. Banert, Organic Azides: Synthesis and Applications, Wiley, Chichester, 2010, 507 pp.
3.

Chapyshev S.V.
Russian Chemical Bulletin,
2011
4.

Chapyshev S.
Molecules,
2015
5.

Yang X., Lin X., Yang L., Zhang T.
Chemical Communications,
2018
6.

Chapyshev S.V., Mendez‐Vega E., Sander W.
Chemistry - A European Journal,
2021
7.

Chapyshev S.V., Korchagin D.V., Misochko E.Y.
Russian Chemical Reviews,
2021
8.

Schmidt L., Wagner D., Nieger M., Bräse S.
Molecules,
2022
9.

Bakulev Vasiliy A., Shafran Yuri M., Beliaev Nikolai A., Beryozkina Tetyana V., Volkova Natalia N., Joy Muthipeedika Nibin, Fan Zhijin
Russian Chemical Reviews,
2022
10.

Tsyrenova Biligma D., Lemport Pavel S., Nenajdenko Valentin G.
Russian Chemical Reviews,
2023
11.

Yakushchenko I.K., Chapyshev S.V.
Russian Chemical Bulletin,
2024
12.

Becker M., Voss K., Villinger A., Schulz A.
Zeitschrift fur Naturforschung - Section B Journal of Chemical Sciences,
2012
13.

Adam D., Holl G., Klap�tke T.M.
Heteroatom Chemistry,
1999
14.
D. Adam, K. Karaghiosoff, T. M. Klapötke, G. Holl, M. Kaiser, Propellants Explos. Pyrotech., 2002, 27, 7; https://doi.org/10.1002/1521-4087(200203)27:1%3C7::AID-PREP7%3E3.0.CO;2-J
15.

Yang W., Lu H., Liao L., Fan G., Ma Q., Huang J.
RSC Advances,
2018
16.

Nikitin S., Diness F.
Chemistry - An Asian Journal,
2024
17.

Misochko E.Y., Akimov A.V., Mazitov A.A., Korchagin D.V., Chapyshev S.V.
Russian Chemical Bulletin,
2012
18.

Chapyshev S.V., Chernyak A.V.
Journal of Fluorine Chemistry,
2013
19.

Olah G.A., Mateescu G.D.
Journal of the American Chemical Society,
1970
20.

Chapyshev S., Chernyak A.
Synthesis,
2012
21.

Chapyshev S.V., Chernyak A.V., Yakushchenko I.K.
Journal of Heterocyclic Chemistry,
2015
22.

Chapyshev S.V., Ushakov E.N., Neuhaus P., Sander W.
Journal of Organic Chemistry,
2014
23.

Chapyshev S.V.
Russian Chemical Bulletin,
2024
24.

Yakushchenko I.K., Chapyshev S.V.
Russian Chemical Bulletin,
2025
25.

Rohrbach S., Smith A.J., Pang J.H., Poole D.L., Tuttle T., Chiba S., Murphy J.A.
Angewandte Chemie - International Edition,
2019
26.

Rossi R.A., Pierini A.B., Peñéñory A.B.
Chemical Reviews,
2002
27.

Gahlot S., Schmitt J., Chevalier A., Villa M., Roy M., Ceroni P., Lehn J., Gingras M.
Chemistry - A European Journal,
2024
28.

Beletskaya I.P., Ananikov V.P.
Chemical Reviews,
2022
29.

Toyoda S., Iizumi K., Yamaguchi J.
Chemical Science,
2025
30.

Sandfort F., Knecht T., Pinkert T., Daniliuc C.G., Glorius F.
Journal of the American Chemical Society,
2020
31.

Sundaravelu N., Sangeetha S., Sekar G.
Organic and Biomolecular Chemistry,
2021
32.

Huang S., Wang M., Jiang X.
Chemical Society Reviews,
2022
33.

Rufino‐Felipe E., Valdés H., Morales‐Morales D.
European Journal of Organic Chemistry,
2022
34.

Mulliken R.S.
Journal of Chemical Physics,
1934
35.

Parr R.G., Szentpály L.V., Liu S.
Journal of the American Chemical Society,
1999
36.

Contreras R.R., Fuentealba P., Galván M., Pérez P.
Chemical Physics Letters,
1999
37.

Pérez P., Toro-Labbé A., Aizman A., Contreras R.
Journal of Organic Chemistry,
2002
38.

Chapyshev S.V., Chernyak A.V., Ushakov E.N.
Magnetic Resonance in Chemistry,
2016
39.

Chapyshev S.V., Ushakov E.N., Chernyak A.V.
Magnetic Resonance in Chemistry,
2013
40.

Chapyshev S.V., Ushakov E.N.
Physical Chemistry Chemical Physics,
2015
41.

Amati M., Stoia S., Baerends E.J.
Journal of Chemical Theory and Computation,
2019
42.

Kwan E.E., Zeng Y., Besser H.A., Jacobsen E.N.
Nature Chemistry,
2018
43.

Lennox A.J.
Angewandte Chemie - International Edition,
2018
44.

Gallardo-Fuentes S., Ormazábal-Toledo R.
New Journal of Chemistry,
2019
45.
M. J. Frisch, G. W. Trucks, H. B. Schlegel, G. E. Scuseria, M. A. Robb, J. R. Cheeseman, G. Scalmani, V. Barone, G. A. Petersson, H. Nakatsuji, X. Li, M. Caricato, A. V. Marenich, J. Bloino, B. G. Janesko, R. Gomperts, B. Mennucci, H. P. Hratchian, J. V. Ortiz, A. F. Izmaylov, J. L. Sonnenberg, D. Williams-Young, F. Ding, F. Lipparini, F. Egidi, J. Goings, B. Peng, A. Petrone, T. Henderson, D. Ranasinghe, V. G. Zakrzewski, J. Gao, N. Rega, G. Zheng, W. Liang, M. Hada, M. Ehara, K. Toyota, R. Fukuda, J. Hasegawa, M. Ishida, T. Nakajima, Y. Honda, O. Kitao, H. Nakai, T. Vreven, K. Throssell, J. A. Montgomery, Jr, J. E. Peralta, F. Ogliaro, M. J. Bearpark, J. J. Heyd, E. N. Brothers, K. N. Kudin, V. N. Staroverov, T. A. Keith, R. Kobayashi, J. Normand, K. Raghavachari, A. P. Rendell, J. C. Burant, S. S. Iyengar, J. Tomasi, M. Cossi, J. M. Millam, M. Klene, C. Adamo, R. Cammi, J. W. Ochterski, R. L. Martin, K. Morokuma, O. Farkas, J. B. Foresman, D. J. Fox, Gaussian 16, revision A.03, Gaussian, Inc., Wallingford, CT, 2016
46.

Zhao Y., Truhlar D.G.
Theoretical Chemistry Accounts,
2007
47.

Marenich A.V., Cramer C.J., Truhlar D.G.
Journal of Physical Chemistry B,
2009
48.

Reed A.E., Weinstock R.B., Weinhold F.
Journal of Chemical Physics,
1985