Keywords
Abstract
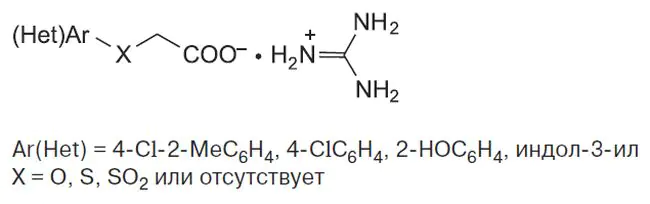
Взаимодействием арилхалькогенилуксусных кислот 1a—e и карбоната гуанидиния 2 синтезированы арилхалькогенилацетаты гуанидиния 3a—e общей формулы ArXCH2COO–•H2+N=C(NH2)2, где X = O, S, SO2 или отсутствует. Строение синтезированных соединений установлено с помощью ИК-спектроскопии и спектроскопии ЯМР 1H и 13C. Расчеты in silico свидетельствуют о том, что соли 3a—e обладают синтетической и биологической доступностью, подобием лекарств, могут эффективно (до 89%) ингибировать активность некоторых ферментов, не обладают иммуно-, цитотоксичностью и мутагенностью (вероятность до 99%), а также практически безвредны (LD50 500 мг•кг–1). Изучено влияние солей 3a—e на рост ряда патогенных бактерий (листерий (Listeria monocytogenes), стафилококков (Staphylococcus aureus), иерсиний (Yersinia enterocolitica, Yersinia pseudotuberculosis, Yersinia pestis) и холерного вибриона (Vibrio cholerae)) in vitro. В высоких концентрациях соли 3a—e оказывают умеренное ингибирующее действие (до 40—50%) на рост микроорганизмов, тогда как в низких концентрациях они проявляют значительную стимулирующую активность (до 82%). Активность солей 3a—e зависит от их строения и состава: максимальная активность наблюдается при ArX = 4-ClC6H4S, 4-ClC6H4SO2 и индол-3-илсульфанил. Серосодержащие соединения улучшают специфическую активность питательных сред, в частности, увеличивают показатель прорастания тест-бактерий (до ∼ 200%).
References