Keywords
Abstract
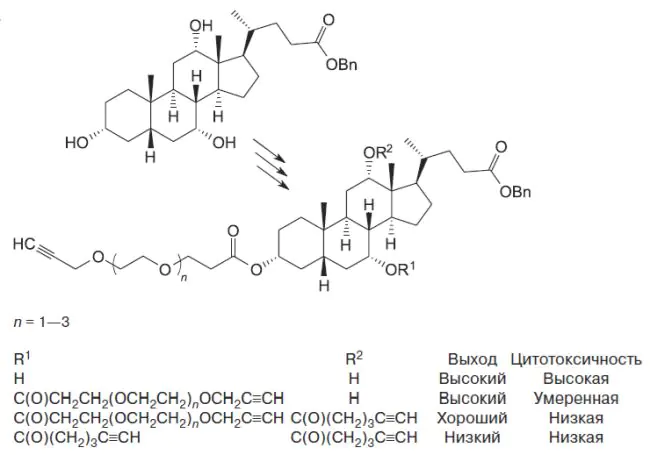
Осуществлен региоселективный синтез гетероантеннарных ацетиленовых производных желчных кислот, содержащих в разных положениях стероидного скелета гекс-5-иноильные, 4,7,10,13-тетраоксагексадец-15-иноильные, 4,7,10-триоксатридец-12-иноильные и 4,7-диоксадец-9-иноильные фрагменты. Исследованы цитотоксические свойства указанных соединений в отношении клеточных линий эмбриональных почек человека HEK293T, фибробластов легких человека VA13, рака груди MCF7 и рака легких A549. Рассчитаны физико-химические параметры синтезированных производных желчных кислот, позволяющие оценить их полярность, общую липофильность и растворимость в воде (TPSA, logP, logS). Установлена корреляция между химическим поведением синтезированных соединений в реакциях этерификации и их биологической активностью. Проведена оценка возможности использования гетероантеннарных продуктов для получения мультивалентных тканеспецифических лигандов и систем направленной доставки лекарств на их основе.
References