Keywords
гетарильные азокрасители
константа связывания
молекулярный докинг
резонансный перенос энергии
сывороточный альбумин
флуоресценция
электронные спектры поглощения
Abstract
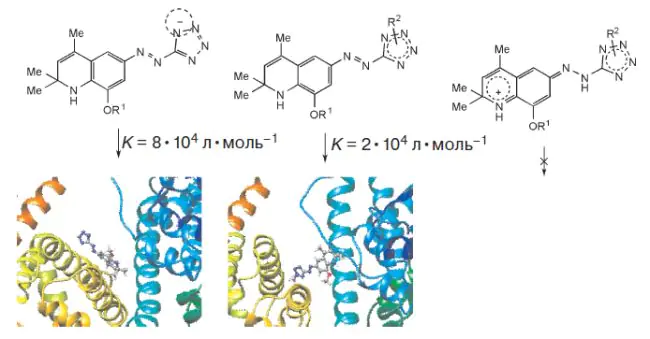
Исследованы процессы комплексообразования новых гетарильных азокрасителей, содержащих дигидрохинолиновый и тетразольный фрагменты, с человеческим сывороточным альбумином (ЧСА). Согласно результатам изучения методом спектрофотометрии в матрице белка эти красители находятся преимущественно в анионной или нейтральной форме в зависимости от строения красителя и pH. Методом тушения флуоресценции ЧСА красителем установлены константы связывания при различных pH, которые зависят от формы красителя и составляют 8.2•104 и (1.3—2.2)•104 л•моль–1 для анионной и нейтральной формы соответственно. Методом молекулярного моделирования определены возможные сайты преимущественного связывания исследуемых красителей.
References
1.

Crespi S., Simeth N.A., König B.
Nature Reviews Chemistry,
2019
2.

Liu Z.F., Hashimoto K., Fujishima A.
Nature,
1990
3.

Ikeda T., Tsutsumi O.
Science,
1995
4.

Broichhagen J., Frank J.A., Trauner D.
Accounts of Chemical Research,
2015
5.

Zhu M., Zhou H.
Organic and Biomolecular Chemistry,
2018
6.
Willner I., Rubin S.
1996
7.

Mart R.J., Allemann R.K.
Chemical Communications,
2016
8.

Wegener M., Hansen M.J., Driessen A.J., Szymanski W., Feringa B.L.
Journal of the American Chemical Society,
2017
9.

Yang X., Ma G., Zheng S., Qin X., Li X., Du L., Wang Y., Zhou Y., Li M.
Journal of the American Chemical Society,
2020
10.

Cabré G., Garrido-Charles A., González-Lafont À., Moormann W., Langbehn D., Egea D., Lluch J.M., Herges R., Alibés R., Busqué F., Gorostiza P., Hernando J.
Organic Letters,
2019
11.

Xia H., Sun Q., Gan N., Ai P., Li H., Li Y.
RSC Advances,
2023
12.
N. Rasouli, N. Sohrabi, D. Ajloo, N. Rezvani, Phys. Chem. Res., 2017, 5, 541; https://doi.org/10.22036/pcr.2017.72343.1343
13.

Zhou X., Li X., Chen X.
Dyes and Pigments,
2013
14.
Li W., Chen F., Wang S.
Protein and Peptide Letters,
2010
15.

Murakami K., Akamatsu M., Sano T.
Bulletin of the Chemical Society of Japan,
1994
16.

Mohanty S., Mishra S.S., Kuldeep, Maharana J., Subuddhi U.
Langmuir,
2024
17.

Zhou X., Lü W., Su L., Shan Z., Chen X.
Journal of Agricultural and Food Chemistry,
2012
19.

Kragh-Hansen U.
Pharmacological Reviews,
1981
20.

Jain A., Judy E., Kishore N.
Journal of Physical Chemistry B,
2024
21.
![pH-Induced Biophysical Perspectives of Binding of Surface-Active Ionic Liquid [BMIM][OSU] with HSA and Dynamics of the Formed Complex](/storage/images/resized/iLiQsFqFaSEx6chlGQ5fbAwF6VYU3WWa08hkss0g_small_thumb.webp)
Ravikanth Reddy R., Saha D., Pan A., Aswal V.K., Mati S.S., Moulik S.P., Phani Kumar B.V.
Langmuir,
2023
22.

Selivanova G.A.
Russian Chemical Bulletin,
2021
23.

Xu Y., Gao C., Andréasson J., Grøtli M.
Organic Letters,
2018
24.

Cameron D., Eisler S.
Journal of Physical Organic Chemistry,
2018
25.

Saylam A., Seferoğlu Z., Ertan N.
Dyes and Pigments,
2008
26.

Samanta S., McCormick T.M., Schmidt S.K., Seferos D.S., Woolley G.A.
Chemical Communications,
2013
27.

Nekipelova T.D., Khodot E.N., Klimovich O.N., Kurkovskaya L.N., Levina I.I., Kuzmin V.A.
Photochemical and Photobiological Sciences,
2016
28.

Nekipelova T.D., Khodot E.N., Deeva Y.S., Levina I.I., Timokhina E.N., Kostyukov A.A., Kuzmin V.A.
Dyes and Pigments,
2021
29.

Khodot E.N., Golovina G.V., Timokhina E.N., Samigullina A.I., Levina I.I., Kuzmin V.A., Nekipelova T.D.
Russian Chemical Bulletin,
2022
30.

Nekipelova T.D., Khodot E.N., Klimovich O.N., Shibaeva A.V., Timokhina E.N., Golovina G.V., Kostyukov A.A., Kuzmin V.A.
Dyes and Pigments,
2022
31.
![Corrigendum to “Dihydroquinolylazotetrazole dyes in aqueous solutions: Effect of substituents and pH on spectral properties, acid-base equilibria and thermal Z‒E isomerization” [Dyes Pigments 199 (2022) 110097] (Dyes and Pigments (2022) 199, (S0143720822000195), (10.1016/j.dyepig.2022.110097))](/storage/images/resized/GDnYOu1UpMMfMMRV6Aqle4H0YLLsraeD9IP9qScG_small_thumb.webp)
Nekipelova T.D., Khodot E.N., Timokhina E.N., Klimovich O.N., Shibaeva A.V., Golovina G.V., Kostyukov A.A., Kuzmin V.A.
Dyes and Pigments,
2023
32.

Golovina G.V., Egorov A.E., Khodot E.N., Kostyukov A.A., Timokhina E.N., Astakhova T.Y., Nekipelova T.D.
Photochemical and Photobiological Sciences,
2023
33.

Hanwell M.D., Curtis D.E., Lonie D.C., Vandermeersch T., Zurek E., Hutchison G.R.
Journal of Cheminformatics,
2012
34.

Morris G.M., Huey R., Lindstrom W., Sanner M.F., Belew R.K., Goodsell D.S., Olson A.J.
Journal of Computational Chemistry,
2009
35.

Trott O., Olson A.J.
Journal of Computational Chemistry,
2009
36.

Pettersen E.F., Goddard T.D., Huang C.C., Couch G.S., Greenblatt D.M., Meng E.C., Ferrin T.E.
Journal of Computational Chemistry,
2004
37.

Vanommeslaeghe K., Hatcher E., Acharya C., Kundu S., Zhong S., Shim J., Darian E., Guvench O., Lopes P., Vorobyov I., Mackerell A.D.
Journal of Computational Chemistry,
2009
38.

Huang J., MacKerell A.D.
Journal of Computational Chemistry,
2013
39.

Abraham M.J., Murtola T., Schulz R., Páll S., Smith J.C., Hess B., Lindahl E.
SoftwareX,
2015
40.

Jo S., Kim T., Iyer V.G., Im W.
Journal of Computational Chemistry,
2008
41.

Lee J., Cheng X., Swails J.M., Yeom M.S., Eastman P.K., Lemkul J.A., Wei S., Buckner J., Jeong J.C., Qi Y., Jo S., Pande V.S., Case D.A., Brooks C.L., MacKerell A.D., et. al.
Journal of Chemical Theory and Computation,
2015
42.

Roe D.R., Cheatham T.E.
Journal of Chemical Theory and Computation,
2013
43.

Salomon-Ferrer R., Case D.A., Walker R.C.
Wiley Interdisciplinary Reviews: Computational Molecular Science,
2012
44.

Shaw A.K., Pal S.K.
Journal of Photochemistry and Photobiology B: Biology,
2008
45.

Mojzisova H., Bonneau S., Vever-Bizet C., Brault D.
Biochimica et Biophysica Acta - Biomembranes,
2007
46.

Mishra P.P., Patel S., Datta A.
Journal of Physical Chemistry B,
2006
47.

Braslavsky S.E., Fron E., Rodríguez H.B., Román E.S., Scholes G.D., Schweitzer G., Valeur B., Wirz J.
Photochemical and Photobiological Sciences,
2008
48.
Н. Л. Векшин, Флуоресцентная спектроскопия биополимеров, Фотон-век, Пущино, 2008, 168 с.
49.

Emel’yanova N.S., Zhilenkov A.V., Pokidova O.V., Gutsev L.G., Zagainova E.A., Sanina N.A., Aldoshin S.M.
Russian Chemical Bulletin,
2024
50.

Milaeva E.R., Shpakovsky D.B., Radchenko E.V., Palyulin V.A., Babkov D.A., Borisov A.V., Dodokhova M.A., Safronenko A.V., Kotieva I.M., Spasov A.A.
Russian Chemical Bulletin,
2022