Keywords
β-амилоид
антиоксиданты
биологическая активность
болезнь Альцгеймера
ферроцен, [1,2,4]триазоло[1,5-а]пиримидин-7-амины
эстеразный профиль
Abstract
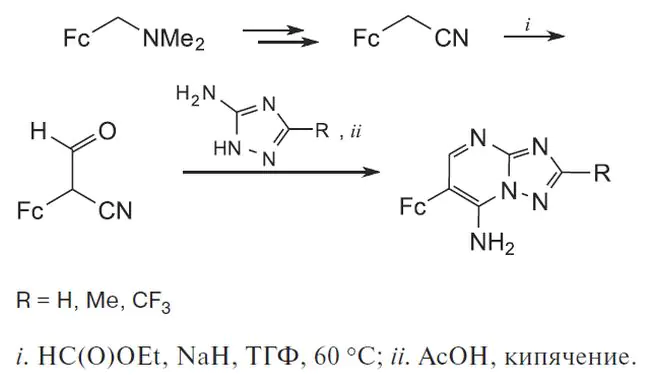
Предложен подход к синтезу неизвестных ранее ферроценилсодержащих [1,2,4]триазоло[1,5-а]пиримидин-7-аминов. α-Формилферроценилацетонитрил вступает в реакцию гетероциклизации с амино-1,2,4-триазолами с образованием целевых соединений с выходами 50—60%. Исследование эстеразного профиля, антиоксидантной активности в тестах АБТС (радикал-связывающая активность) и FRAP (железо-восстанавливающая активность), а также антиагрегационной активности в отношении β-амилоида (ингибирование АХЭ-индуцируемой и самоагрегации β-амилоида) полученных конъюгатов показало, что ферроценилсодержащие [1,2,4]триазоло[1,5-а]пиримидин-7-амины перспективны для создания мультифункциональных препаратов для лечения болезни Альцгеймера.
References
1.

Benek O., Korabecny J., Soukup O.
Trends in Pharmacological Sciences,
2020
2.

Mesiti F., Chavarria D., Gaspar A., Alcaro S., Borges F.
European Journal of Medicinal Chemistry,
2019
3.
Pasieka A., Panek D., Malawska B.
2020
4.

Tahami Monfared A.A., Byrnes M.J., White L.A., Zhang Q.
Neurology and Therapy,
2022
5.
Carreiras M., Mendes E., Perry M., Francisco A., Marco-Contelles J.
Current Topics in Medicinal Chemistry,
2013
6.

Edwards E.I., Epton R., Marr G.
Journal of Organometallic Chemistry,
1975
7.

Edwards E.I., Epton R., Marr G.
Journal of Organometallic Chemistry,
1976
8.

Edwards E.I., Epton R., Marr G.
Journal of Organometallic Chemistry,
1979
9.

Patra M., Gasser G., Wenzel M., Merz K., Bandow J.E., Metzler-Nolte N.
Organometallics,
2010
10.

Patra M., Gasser G., Metzler-Nolte N.
Dalton Transactions,
2012
11.

Mu C., Prosser K.E., Harrypersad S., MacNeil G.A., Panchmatia R., Thompson J.R., Sinha S., Warren J.J., Walsby C.J.
Inorganic Chemistry,
2018
12.

Wang R., Chen H., Yan W., Zheng M., Zhang T., Zhang Y.
European Journal of Medicinal Chemistry,
2020
13.

Gadhachanda V.R., Eastman K.J., Wang Q., Phadke A.S., Patel D., Yang W., Marlor C.W., Deshpande M., Huang M., Wiles J.A.
Bioorganic and Medicinal Chemistry Letters,
2018
14.

Pejović A., Minić A., Jovanović J., Pešić M., Komatina D.I., Damljanović I., Stevanović D., Mihailović V., Katanić J., Bogdanović G.A.
Journal of Organometallic Chemistry,
2018
15.

Stringer T., Wiesner L., Smith G.S.
European Journal of Medicinal Chemistry,
2019
16.

Zyryanova E.Y., Utepova I.A., Musikhina A.A., Boltneva N.P., Kovaleva N.V., Rudakova E.V., Serebryakova O.G., Makhaeva G.F., Kiskin M.A., Lazarev V.F., Kuznetsova L.S., Guzhova I.V., Chupakhin O.N.
Russian Chemical Bulletin,
2024
17.

Kumar Singh P., Silakari O.
Journal of Biomolecular Structure and Dynamics,
2018
18.

Aroua L.M., Alkhaibari I.S., Alminderej F.M., Messaoudi S., Chigurupati S., Al-mahmoud S., Albadri A.E., Emwas A., Mohammed H.H.
Journal of Molecular Structure,
2025
19.
Journal of Applied Pharmaceutical Science,
2017
20.

Goyal D., Shuaib S., Mann S., Goyal B.
ACS Combinatorial Science,
2017
21.

Yao P., Zhang J., You S., Qi W., Su R., He Z.
Journal of Materials Chemistry B,
2020
22.

Altaf A.A., Hamayun M., Lal B., Tahir M.N., Holder A.A., Badshah A., Crans D.C.
Dalton Transactions,
2018
23.

Jawaria R., Hussain M., Ahmad H.B., Ashraf M., Hussain S., Naseer M.M., Khalid M., Hussain M.A., al-Rashida M., Tahir M.N., Asim S., Shafiq Z.
Inorganica Chimica Acta,
2020
24.

Halder B., Mitra A., Dewangan S., Gazi R., Sarkar N., Jana M., Chatterjee S.
Journal of Molecular Structure,
2023
25.

Larik F.A., Saeed A., Fattah T.A., Muqadar U., Channar P.A.
Applied Organometallic Chemistry,
2016
26.

Snegur L.V.
Inorganics,
2022
27.

Singh P.K., Choudhary S., Kashyap A., Verma H., Kapil S., Kumar M., Arora M., Silakari O.
Bioorganic Chemistry,
2019
28.

Renyu Q., Yuchao L., Kandegama W.M., Qiong C., Guangfu Y.
Mini-Reviews in Medicinal Chemistry,
2018
29.

Kumar J., Meena P., Singh A., Jameel E., Maqbool M., Mobashir M., Shandilya A., Tiwari M., Hoda N., Jayaram B.
European Journal of Medicinal Chemistry,
2016
30.
![Synthesis and Biological Investigation of 1,2,4-Triazolo[4,3-a]azines as Potential HSF1 Inductors](/storage/images/resized/xqixcltwJYe6H8Uco2JbAFfIOzt7UNKH0OcPOPzO_small_thumb.webp)
Utepova I.A., Serebrennikova P.O., Chupakhin O.N., Guzhova I.V., Mikhaylova E.R., Antonchick A.P.
Synthesis,
2022
31.

Makhaeva G.F., Rudakova E.V., Kovaleva N.V., Lushchekina S.V., Boltneva N.P., Proshin A.N., Shchegolkov E.V., Burgart Y.V., Saloutin V.I.
Russian Chemical Bulletin,
2019
32.

Biot C., Delhaes L., Abessolo H., Domarle O., Maciejewski L.A., Mortuaire M., Delcourt P., Deloron P., Camus D., Dive D., Brocard J.S.
Journal of Organometallic Chemistry,
1999
33.

Ripert M., Farre C., Chaix C.
Electrochimica Acta,
2013
34.

Ellman G.L., Courtney K.D., Andres V., Featherstone R.M.
Biochemical Pharmacology,
1961
35.

Makhaeva G.F., Kovaleva N.V., Boltneva N.P., Lushchekina S.V., Astakhova T.Y., Rudakova E.V., Proshin A.N., Serkov I.V., Radchenko E.V., Palyulin V.A., Bachurin S.O., Richardson R.J.
Molecules,
2020
36.

Taylor P., Lappi S.
Biochemistry,
1975
37.

Biancalana M., Koide S.
Biochimica et Biophysica Acta - Proteins and Proteomics,
2010
38.
![[18] Quantification of β-sheet amyloid fibril structures with thioflavin T](/storage/images/resized/GDnYOu1UpMMfMMRV6Aqle4H0YLLsraeD9IP9qScG_small_thumb.webp)
LeVine H.
Methods in Enzymology,
1999
39.

Muñoz-Ruiz P., Rubio L., García-Palomero E., Dorronsoro I., del Monte-Millán M., Valenzuela R., Usán P., de Austria C., Bartolini M., Andrisano V., Bidon-Chanal A., Orozco M., Luque F.J., Medina M., Martínez A., et. al.
Journal of Medicinal Chemistry,
2005
40.

Re R., Pellegrini N., Proteggente A., Pannala A., Yang M., Rice-Evans C.
Free Radical Biology and Medicine,
1999
41.

Makhaeva G.F., Kovaleva N.V., Boltneva N.P., Lushchekina S.V., Rudakova E.V., Stupina T.S., Terentiev A.A., Serkov I.V., Proshin A.N., Radchenko E.V., Palyulin V.A., Bachurin S.O., Richardson R.J.
Bioorganic Chemistry,
2020
42.

43.

Makhaeva G.F., Kovaleva N.V., Rudakova E.V., Boltneva N.P., Lushchekina S.V., Faingold I.I., Poletaeva D.A., Soldatova Y.V., Kotelnikova R.A., Serkov I.V., Ustinov A.K., Proshin A.N., Radchenko E.V., Palyulin V.A., Richardson R.J., et. al.
Molecules,
2020