Keywords
Abstract
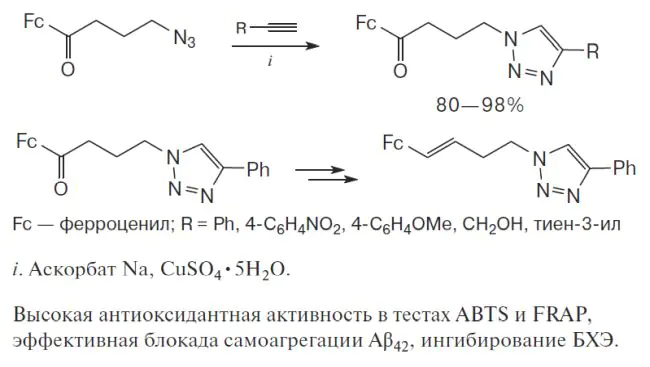
Путем Cu-катализируемого азид-алкинового циклоприсоединения получен ряд новых ферроценовых конъюгатов, содержащих 1Н-1,2,3-триазольные фрагменты. Исследована биологическая активность соединений как потенциальных лекарственных препаратов для терапии сопутствующих мультифакторных заболеваний — болезни Альцгеймера и сахарного диабета второго типа. Исследование включало определение эстеразного профиля, оценку способности ингибирования самоагрегации β-амилоида (1-42) и оценку собственной антиоксидантной активности соединений. Для синтезированных конъюгатов показана высокая радикал-связывающая способность в тесте АБТС и железо-восстанавливающая способность в тесте FRAP, а также высокая ингибирующая активность в отношении самоагрегации β-амилоида (1-42) и умеренное ингибирование бутирилхолинэстеразы.
References















![Novel ferrocene-pyrazolo[1,5-a]pyrimidine hybrids: A facile environment-friendly regioselective synthesis, structure elucidation, and their antioxidant, antibacterial, and anti-biofilm activities](/storage/images/resized/voXLqlsvTwv5p3iMQ8Dhs95nqB4AXOG7Taj7G4ra_small_thumb.webp)


























![[18] Quantification of β-sheet amyloid fibril structures with thioflavin T](/storage/images/resized/GDnYOu1UpMMfMMRV6Aqle4H0YLLsraeD9IP9qScG_small_thumb.webp)