Keywords
биомолекулы
взаимодействие мишень—лиганд
количественное соотношение структура—активность (QSAR)
медицинская химия
моделирование структуры фармакофора
молекулярный докинг
Abstract
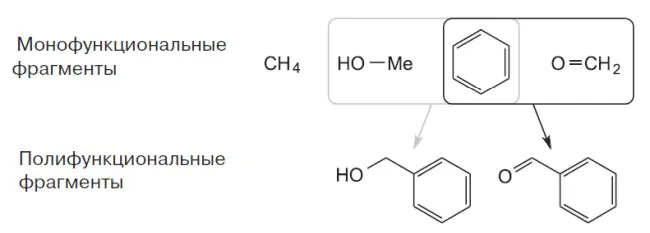
В работе сформированы и апробированы на нескольких наборах фрагментов, в том числе предложенных авторами, критерии отбора и сравнения молекул и самих наборов для последующего исследования мишени и моделирования структуры фармакофора. Ключевые требования к фрагментам и критерии оценки их эффективности для дальнейшего моделирования фармакофора оформлены и закреплены в концепции фрагментных базисов — минимальных наборов зондирующих молекул или их фрагментов, максимально покрывающих основные типы взаимодействий мишень—лиганд.
References
1.

Wermuth C.G., Ganellin C.R., Lindberg P., Mitscher L.A.
Pure and Applied Chemistry,
1998
2.
О. Н. Зефирова, К. В. Балакин, М. Ю. Красавин, В. А. Палюлин, В. В. Поройков, Е. В. Радченко, Н. Ф. Салахутдинов, А. А. Спасов, В. П. Фисенко, С. О. Бачурин, Изв. АН. Сер. хим., 2019, 68, 2381
3.

Choudhury C., Narahari Sastry G.
Challenges and Advances in Computational Chemistry and Physics,
2019
4.

Shulga D.A., Shaimardanov A.R., Ivanov N.N., Palyulin V.A.
International Journal of Molecular Sciences,
2022
5.

Costa P.J., Nunes R., Vila-Viçosa D.
Expert Opinion on Drug Discovery,
2019
6.

7.

Dixon S.L., Smondyrev A.M., Knoll E.H., Rao S.N., Shaw D.E., Friesner R.A.
Journal of Computer-Aided Molecular Design,
2006
8.

Barnum D., Greene J., Smellie A., Sprague P.
Journal of Chemical Information and Computer Sciences,
1996
9.

Chang Y., Hawkins B.A., Du J.J., Groundwater P.W., Hibbs D.E., Lai F.
Pharmaceutics,
2022
10.

Wolber G., Langer T.
Journal of Chemical Information and Modeling,
2004
11.

Sanders M.P., McGuire R., Roumen L., de Esch I.J., de Vlieg J., Klomp J.P., de Graaf C.
MedChemComm,
2012
12.

Kapingidza A.B., Kowal K., Chruszcz M.
Sub-Cellular Biochemistry,
2020
13.

Schaller D., Šribar D., Noonan T., Deng L., Nguyen T.N., Pach S., Machalz D., Bermudez M., Wolber G.
Wiley Interdisciplinary Reviews: Computational Molecular Science,
2020
14.

Friesner R.A., Murphy R.B., Repasky M.P., Frye L.L., Greenwood J.R., Halgren T.A., Sanschagrin P.C., Mainz D.T.
Journal of Medicinal Chemistry,
2006
15.

Salam N.K., Nuti R., Sherman W.
Journal of Chemical Information and Modeling,
2009
16.

Goodford P.J.
Journal of Medicinal Chemistry,
1985
17.

Baroni M., Cruciani G., Sciabola S., Perruccio F., Mason J.S.
Journal of Chemical Information and Modeling,
2007
18.

Morris G.M., Huey R., Lindstrom W., Sanner M.F., Belew R.K., Goodsell D.S., Olson A.J.
Journal of Computational Chemistry,
2009
19.

Di Stefano M., Galati S., Piazza L., Gado F., Granchi C., Macchia M., Giordano A., Tuccinardi T., Poli G.
Journal of Enzyme Inhibition and Medicinal Chemistry,
2024
20.
Medvedev M.G., Stroganov O.V., Dmitrienko A.O., Panova M.V., Lisov A.A., Svitanko I.V., Novikov F.N., Chilov G.G.
Mendeleev Communications,
2022
21.

Egorov M.P., Ananikov V.P., Baskir E.G., Boganov S.E., Bogdan V.I., Vereshchagin A.N., Vil’ V.A., Dalinger I.L., Dilman A.D., Eliseev O.L., Zlotin S.G., Knyazeva E.A., Kogan V.M., Kononov L.O., Krayushkin M.M., et. al.
Russian Chemical Bulletin,
2024
22.

Tyukina S.P., Velmiskina J.A., Dmitrienko A.O., Medvedev M.G.
Journal of Physical Chemistry Letters,
2024
23.

Peterson A.A., Liu D.R.
Nature Reviews Drug Discovery,
2023
24.

Xu W., Kang C.
Journal of Medicinal Chemistry,
2025
25.

Kirkman T., dos Santos Silva C., Tosin M., Bertacine Dias M.V.
ChemMedChem,
2024
26.

Ngan C., Hall D.R., Zerbe B., Grove L.E., Kozakov D., Vajda S.
Bioinformatics,
2011
27.

Heider J., Kilian J., Garifulina A., Hering S., Langer T., Seidel T.
Journal of Chemical Information and Modeling,
2022
28.

Wishart D.S., Feunang Y.D., Guo A.C., Lo E.J., Marcu A., Grant J.R., Sajed T., Johnson D., Li C., Sayeeda Z., Assempour N., Iynkkaran I., Liu Y., Maciejewski A., Gale N., et. al.
Nucleic Acids Research,
2017
29.

Berthold M.R., Cebron N., Dill F., Gabriel T.R., Kötter T., Meinl T., Ohl P., Thiel K., Wiswedel B.
ACM SIGKDD Explorations Newsletter,
2009
30.
RDKit Molecule Fragmenter; RDKit Nodes Feature; https://hub.knime.com/manuelschwarze/extensions/org.rdkit.knime.feature/latest/org.rdkit.knime.nodes.molfragmenter.RDKitMolFragmenterNodeFactory (дата обращения: 01.02.2025)
31.

Ivanov N.N., Shulga D.A., Palyulin V.A.
Biophysica,
2023
32.
G. Landrum, P. Tosco, B. Kelley, R. Rodriguez, D. Cosgrove, R. Vianello, sriniker, P. Gedeck, G. Jones, N. Schneider, E. Kawashima, D. Nealschneider, A. Dalke, M. Swain, B. Cole, S. Turk, A. Savelev, tadhurst-cdd, A. Vaucher, M. Wójcikowski, I. Take, R. Walker, V.F. Scalfani, K.Ujihara, D. Probst, J. Lehtivarjo, H. Faara, guillaume godin, A. Pahl, J. Monat, Zenodo, 2025, 21.03.2025
33.
RDKit Canon SMILES; RDKit Nodes Feature; https://hub.knime.com/manuelschwarze/extensions/org.rdkit.knime.feature/latest/org.rdkit.knime.nodes.canonsmiles.RDKitCanonicalSmilesNodeFactory (дата обращения: 01.02.2025)
34.
RDKit Descriptor Calculation, RDKit Nodes Feature; https://hub.knime.com/manuelschwarze/extensions/org.rdkit.knime.feature/latest/org.rdkit.knime.nodes.descriptorcalculation.DescriptorCalculationNodeFactory (дата обращения: 01.02.2025)
35.
RDKit Nodes Feature; https://hub.knime.com/manuelschwarze/extensions/org.rdkit.knime.feature/latest/ (дата обращения: 01.02.2025)
36.

Nguyen K., Blum L., van Deursen R., Reymond J.
ChemMedChem,
2009
37.

Wildman S.A., Crippen G.M.
Journal of Chemical Information and Computer Sciences,
1999
38.

Ertl P., Rohde B., Selzer P.
Journal of Medicinal Chemistry,
2000